Brasil/Mundo
Ministério da Saúde bloqueia distribuição de lotes suspensos da CoronaVac
Pasta também determinou que pessoas imunizadas com os compostos embargados sejam monitoradas por 30 diasO Ministério da Saúde bloqueou a distribuição das mais de 12 milhões de doses da vacina CoronaVac envasadas na China em uma fábrica não certificada pela Agência Nacional de Vigilância Sanitária (Anvisa). A medida busca evitar que as vacinas sejam movimentadas até que haja definição da agência. Sem detalhar, a pasta da saúde também determinou que as pessoas imunizadas com os lotes embargados sejam monitoradas por 30 dias. Em reunião na segunda-feira (6), o Instituto Butantan apresentou à Anvisa um documento que conclui que não há risco nas unidades da CoronaVac interditadas na semana passada. No entanto, a entidade não entregou relatórios que comprovem as Boas Práticas de fabricação de unidades envolvidas, solicitados pela agência. Em nota, o Butantan explicou que, por questões internas da autoridade sanitária chinesa, o conteúdo não pôde ser disponibilizado diretamente ao Instituto.
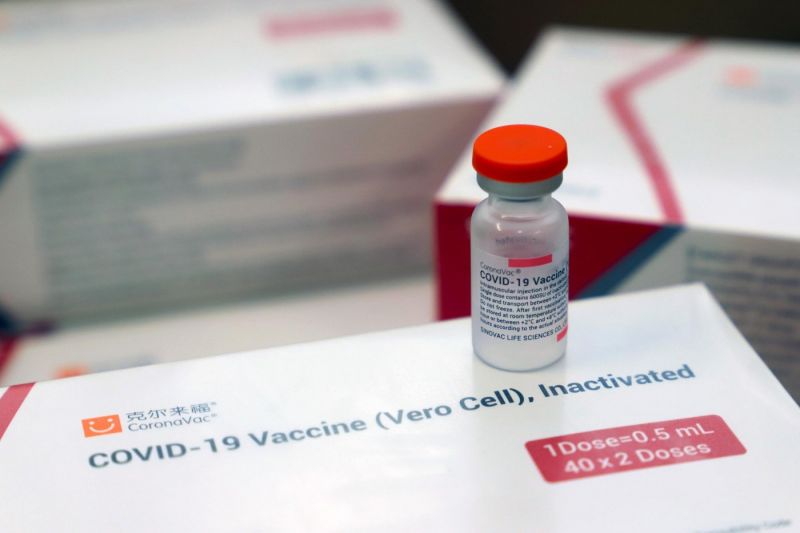 Segundo o Instituto Butantan, todos os lotes da CoronaVac passaram por um rigoroso controle de qualidade no Brasil. Foto: Roberto Vazquez | Estadão Conteúdo
Segundo o Instituto Butantan, todos os lotes da CoronaVac passaram por um rigoroso controle de qualidade no Brasil. Foto: Roberto Vazquez | Estadão Conteúdo
A equipe teve acesso apenas aos dados das não conformidades observadas e ao plano de ação proposto para ajustar os problemas. Com isso, o Butantan sugeriu que a Anvisa faça uma inspeção remota às plantas. A agência, por outro lado, afirma que o método apresenta “limitações e dificuldades, como barreiras linguísticas e filmagem não adequada das áreas fabris”. O órgão iniciou, internamente, os processos para uma eventual inspeção presencial às unidades. Em nota, o Instituto ressaltou que a fábrica chinesa tem certificação que segue boas práticas internacionais e que todos os lotes da CoronaVac passaram por um rigoroso controle de qualidade no Brasil.
Utilize o formulário abaixo para comentar.
-
09/05/2026 07:29
Mudanças na lei ampliam acesso ao salário-maternidade; entenda as novas regras
Sem exigência mínima de 10 meses, benefício alcança mais mulheres e orientação adequada pode auxiliar na busca pelo direito
-
06/02/2026 12:55
De Alagoas para a China, empresa de mel está levando a caatinga para o mercado asiático
Presente em grandes redes do varejo a beeva fortalece a apicultura do semiárido e amplia negócios com a China.
-
01/01/2026 11:06
Mega da Virada 2025: CAIXA divulga dezenas do prêmio histórico de R$ 1,09 bilhão
Sorteio foi adiado por problemas técnicos e números foram revelados na manhã do primeiro dia de 2026
-
31/12/2025 23:58
Caixa adia sorteio da Mega da Virada para esta quinta-feira; valor será de R$ 1,09 bilhão
A Caixa informou que o sorteio da Mega da Virada 2025 foi adiado para esta quinta-feira, 1° de janeiro, às 10h, em razão da necessidade de ajustes operacionais.
-
29/12/2025 14:16
Bolsonaro passa por segundo procedimento médico para tratar soluços persistentes
Ele passa por uma intervenção chamada de 'bloqueio do nervo frênico'. Desta vez, no nervo do lado direito.
-
Mandado cumprido
Acusado de estuprar idosa de 81 anos é preso em cumprimento de mandado em Delmiro Gouveia
-
Danos causados
Suspeitos fogem após tentarem furtar máquina compactadora em Delmiro Gouveia
-
Acidente
Homem é hospitalizado após cair da garupa de moto em Delmiro Gouveia
-
Danos materiais
Entregador delivery colide moto com micro-ônibus da educação em Delmiro Gouveia
Interessa a você
 Dólar5,28895,29190.0052
Dólar5,28895,29190.0052 Euro6,17906,2290-0.071
Euro6,17906,2290-0.071Blogs
-
Haroldo Almeida Ygo Costa é nomeado como Secretário de Meio Ambiente de Alagoas e Participa de Oficina TEJET

-
Senadinho A oposição que vive do passado e tenta sabotar o presente em Olho D’água do Casado

-
Wellington Amâncio Noite dos Escritores Delmirenses

-
Jota Silva Marcos Costa se coloca à disposição de Ziane para disputa em 2028 em Delmiro Gouveia

CNTV
-
Caso Cícero Rosa
Polícia já sabe quem matou vigilante em Inhapi e investiga motivação do crime
-
Investigação
Promotor de Justiça fala sobre morte de policiais civis em Delmiro Gouveia
-
Caso Evilly Soares
Polícia Civil amplia investigação sobre morte de jovem em Maravilha
-
Tragédia na AL-220
Polícia Civil descarta falha mecânica em acidente com ônibus em São José da Tapera
Enquete
Você está satisfeito com o vereador ou vereadora em quem votou na última eleição?
Últimas Notícias
-
1
Polícia registra caso de perturbação do sossego envolvendo criança com autismo em Piranhas
-
2
Homem sem habilitação é flagrado fazendo manobras perigosas em povoado de Pariconha
-
3
Acusado de estuprar idosa de 81 anos é preso em cumprimento de mandado em Delmiro Gouveia
-
4
Motorista bate em carro estacionado ao se distrair com bolo para surpresa da filha em escola
-
5
Piranhas: Tiago Freitas e Inácio Loiola fortalecem parceria pela regularização fundiária rural
Mais Acessadas
-
1
Homem é morto a tiros enquanto conduzia moto por estrada vicinal em Inhapi
-
2
Policiais civis são mortos a tiros por colega enquanto retornavam de missão em Delmiro Gouveia
-
3
Policial civil teria dito que cochilou antes de ter atirado nos colegas de equipe em Delmiro
-
4
Duas mulheres são presas em flagrante por perturbação do sossego em povoado de Pariconha
-
5
Mulher morre vítima de atropelamento em trecho da rodovia BR-423 em Delmiro Gouveia
Mais Comentadas
-
1
TRE manda Zé Hermes e filho removerem vídeo por desinformação contra grupo de Celso Luiz
-
2
Ronaldo Lessa pode fazer dobradinha com Renan Calheiros para o Senado
-
3
Policial civil teria dito que cochilou antes de ter atirado nos colegas de equipe em Delmiro
-
4
Gestão Tiago Freitas coloca Piranhas em 1º lugar entre municípios com melhor qualidade de
-
5
Comerciante com passagens por roubo a banco é apontado como mandante da morte de Cícero Rosa














